

私たちが病気やけがをしたとき、多くは「薬」を使って治療が行われます。薬は効果があり、副作用が少ないことが重要です。
新しい薬が世の中に出てくるためには、最初に「薬」になる可能性のある物質について試験管内での作用を調べます。
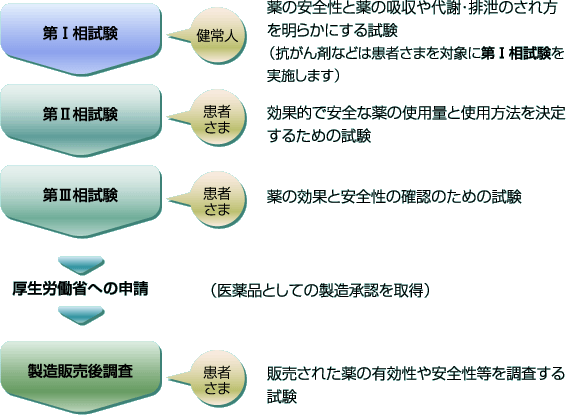
次に、薬として役に立つ候補の物質だけを動物に使用して、どのような作用があるかを調べます。そのうち、薬として役に立ち、なおかつ副作用が少ないと考えられる物質のみを、健康な人のご協力を得て使用していただき、どのように身体に吸収されたり排泄されたりするのか、どのような副作用がどのくらいあるのかを確認します。

その結果、安全性が確認されたものを、患者さまのご協力を得て使用していただき、人の病気の治療にどのくらい役立つのか、副作用がどのくらいあるのかを確認します。
このため、製薬企業は病院に依頼して、新しい薬の候補が病気の治療に有用かどうかを調べています。製薬企業はそれらの結果をまとめて厚生労働省に提出し、厚生労働省はその結果について厳格な審査を行った上で、医薬品として有用性のあるものを承認します。
そしてはじめて、多くの患者さまに医薬品として広くご使用いただくことができるようになります。

このように、医薬品の開発段階で健康な人や患者さまに実際に「薬」をご使用いただいて、効果と安全性を確かめる臨床試験を「治験」といい、治験で使われる薬を「治験薬」といいます。また厚生労働省から承認を受けて医薬品が販売された後も、製薬企業はその医薬品のさらなる有効性や安全性の情報を集めるために「製造販売後調査」を行います。製造販売後調査の中で、日常診療として行う検査以外の検査を行ったり、他の薬と比較を行ったりして、その結果を詳しく調べる試験を「製造販売後臨床試験」といいます。
したがって、治験や製造販売後臨床試験は患者さまの治療であるとともに、試験を目的とするものでもあります。


治験や製造販売後臨床試験は国が定めた「薬事法」や「医薬品の臨床試験の実施の基準(GCP)」、「医薬品の製造販売後の調査及び試験の実施(GPSP)」などの法律を守って実施されています。
また、病院長が病院内に治験審査委員会という委員会を設置し、患者さまの安全等を守る立場から、新しい治験を実施する場合はその内容が科学的および倫理的に適正かどうか、新たな情報などを入手した場合はその治験を継続しても問題ないかどうか、その委員会が調査および審査を行い、その審査結果を基に病院長に意見を述べます。治験審査委員会の意見に基づいて、病院長がその治験の実施や継続を決定します。






