

くすりの候補(治験薬)を使うことで、病気や症状の改善が期待できると担当医師が判断した患者さまに、治験の参加についてお話させていただきます。

まずはじめに、治験を担当する医師やCRC(Clinical Research Coordinator:臨床研究コーディネーター)が、治験に関するくわしい説明をいたします。その時には治験の目的や方法、検査の内容、来院回数や、その治験薬(薬の候補)の、予測される効き目と副作用などが書かれた説明書 ─これを同意説明文書といいます─ をお渡しします。
ここで疑問点があれば、治験を担当する医師に対して、納得のいくまで説明を求めてください。![]() インフォームド・コンセントってなに?
インフォームド・コンセントってなに?

治験の内容をご理解いただけて、治験に参加されることにご納得いただけましたら、同意書に署名と日付けをご記載ください。
もちろん、その場でお決めいただかなくても構いません。同意説明文書をお持ち帰りいただき、ご家族やお友だちと相談されるなど、十分に検討されてからでもかまいません。その後に説明をした医師にご自身の意思をお伝えください。
参加基準は治験の内容によって異なります。
治験の対象となる病気の程度や、これまでの経過、他の病気の状況、決められた時期に通院が可能なこと、また、年齢や性別などが、治験ごとに詳しく決められています。
治験への参加にご同意いただけた方には、その治験の基準に合致されるかどうかを調べる診察や検査を行ないます。その結果によっては、参加者ご本人が希望されても、参加いただけない場合があります。
治験を担当する医師から指示された用法・用量を守って、一定期間、治験薬をご使用いただきます。プラセボを使用する治験もあります。![]() プラセボってなに?
プラセボってなに?

治験の内容によっては通常よりも来院回数が増えることもあります。また、治験に参加中は採血、採尿、血圧測定などの検査を実施して、病状の回復具合だけではなく体調の変化も詳しく調べます。
もちろん、参加者ご本人が体調の変化を感じられましたら、すぐに治験を担当する医師、または相談窓口にご連絡ください。

「インフォームド・コンセント」とは、患者さまが治療を受ける前に病気のことや治療方法などについて、医師等から十分な説明を受け、患者さまがその説明の内容をよく理解し納得したうえで、患者さま自身の意思で治療を受けることに同意することを言います。
治験におけるインフォームド・コンセントは、治験を行う医師が患者さまに治験の目的や実施方法、治験薬の有効性と安全性などが書かれた「同意説明文書」をもとに、その治験についての内容を詳しく説明し、理解していただきます。ここで患者さまが参加することに同意されて、はじめて治験が開始されます。
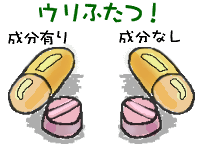
プラセボとは、見た目や味・匂いなどが、治験薬と全く同じで、薬の有効成分だけが入っていないもののことです。治験薬の有効性や副作用が、自然治癒力や先入観に左右されず、正しく判断するために使われます。

治験薬の成分が入ったものと成分の入っていないもの(プラセボ)を比較する治験の場合は、正しく判断するために、どちらを飲んでいるのか、医師や患者さま、担当CRCにも分からないようになっています。この方法はお薬の有効性などを調べる場合、世界中で使用されている試験方法のひとつです。














