生理学分野
生理学は、正常な生命現象の機能を理解し病理現象や臨床各科を学ぶための基礎となる学問です。また同時に「未来を拓く学問」であるとも言えます。近年注目される再生医学、医工連携といった先端研究は、失われた人体機能を生理的な状態に回復することを目的としています。再生した組織や人工的に作り出した臓器は、私たちの体と連携して新しい機能的な生理状態を作り出すことになります。私たちの教室ではこれらの「新しい人体生理」を理解するため、特に細胞間コミュニケーションについて研究しています。
研究グループ
- エクソソーム/ナノチューブ
エクソソーム/ナノチューブを介した細胞間コミュニケーションの解析 - ペプチドシグナル
生体内ペプチドシグナルの解析と臨床応用を目指したトランスレーショナル研究 - ストレスシグナル
新しいストレスマーカーの開発と細胞間情報伝達メカニズムの解明 - 細胞移植
羊膜上皮細胞を用いた細胞治療の臨床応
<エクソソーム/ナノチューブ>
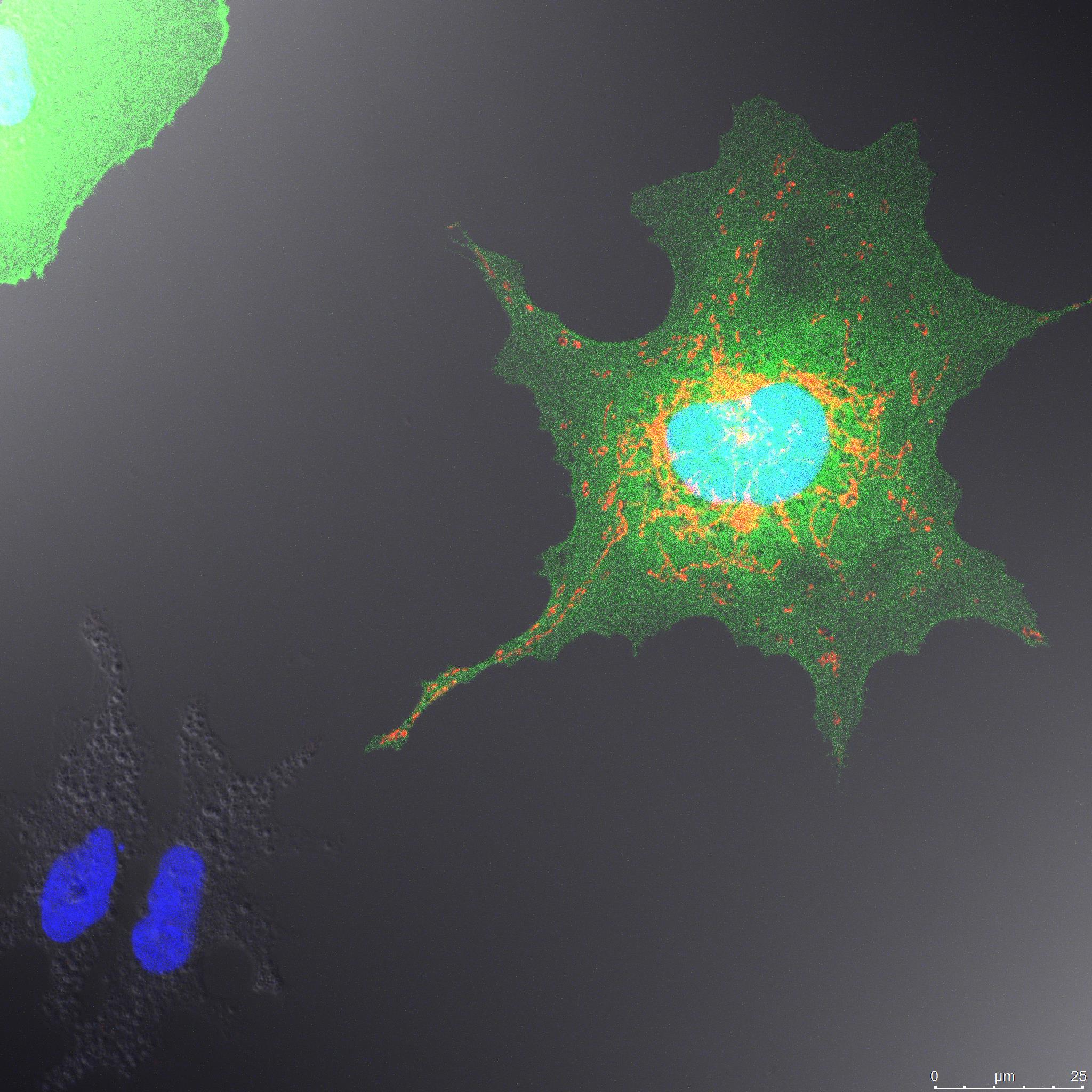
多細胞生物である私たちの細胞は、常に近隣のまた遠く離れた他の細胞と情報交換をして恒常性を保っています。よく知られている神経系や内分泌系の情報伝達システムに加え近年新しい情報伝達システムがあることがわかってきました。私たちは、細胞移植という手法を使うことによって 情報を発信している細胞と受け取る細胞を可視化することができるのではないかと考えました。細胞小器官やタンパク質を蛍光ラベルすることによって これまでは調べることができなかった興味深い現象の詳細を明らかにすることができます。私たちは、エクソソームを使った遠距離での細胞間伝達や、ナノチューブを介した近距離での細胞間伝達に注目しています。次の写真は、蛍光色素で細胞質を緑に、ミトコンドリアを赤に染めた羊膜上皮細胞が近隣の細胞にミトコンドリアを分配する現象を捉えたものです。このような蛍光ラベル技術と細胞移植をツールとして使うことで、細胞間情報伝達の様々な新しい発見につながるのではないかと考えています。
<ペプチドシグナル>
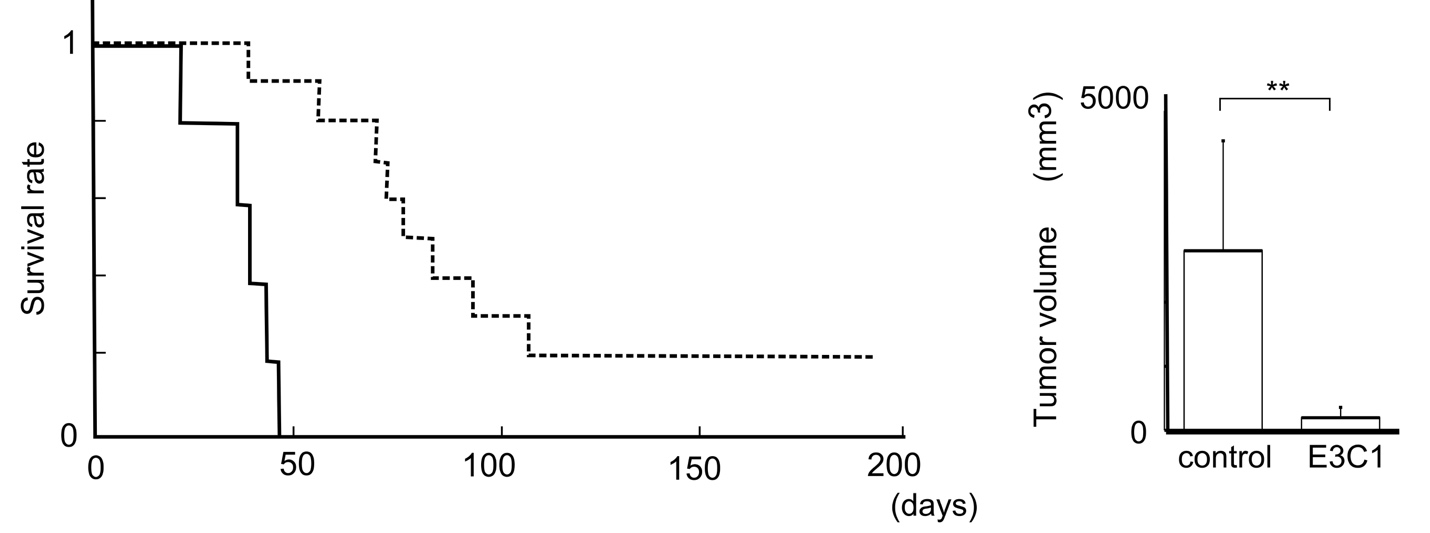
ペプチドとは、100個以下のアミノ酸が重合したものであり、様々な生理活性を持つ細胞間情報伝達物質の一つです。私たちは、血液凝固第IX因子としてよく知られたタンパクが凝固止血以外に、細胞に対する種々の作用を持つことを明らかにしてきました。第IX因子のEGFドメインは、凝固反応の過程で活性化され、アポトーシスを誘導する作用があります。このドメインと相同性が高く、同じ機能をもつEGFドメインは、30強のタンパクに共有されています。このEGFドメインをコードするDNAを用いて担癌モデルマウスの遺伝子治療を行ったところ、腫瘍増殖は抑制され、生命予後も改善しました。一方、凝固反応時に切除されるペプチドには、内皮細胞の透過性を抑制する作用があることがわかりました。敗血症、脳梗塞、脳外傷等の動物モデルでは当該ペプチドの投与により組織の浮腫が減少し、予後が改善したり、梗塞巣が縮小したりしました。これらのペプチドは元来人体に存在するため、化学物質のような副作用は現れません。私たちはこれらのペプチドを治療剤として実用化するべく、研究を続けています。
<ストレスシグナル>
私たちは、苦味を感じる味覚受容体タンパクの一つであるTAS2Rファミリーの遺伝子発現が、ストレスレベルに応じて変化することを発見しました。また、この遺伝子は舌の細胞だけではなく脳をはじめとするいろいろな細胞に発現していることも明らかにしました。しかし、どうして味覚受容体タンパクが舌以外の組織に発現しているのか、どうやってストレスシグナルがこの遺伝子発現を調節しているのか、また遠く離れたTAS2Rファミリーの遺伝子発現は全てストレスレベルに同調しているのかなど、まだ分かっていないことが多くあります。私たちは、このメカニズムを明らかにすることによって、乳児や意識のない患者さんのストレスレベルを非侵襲的に定量化する技術の開発に取り組んでいます。
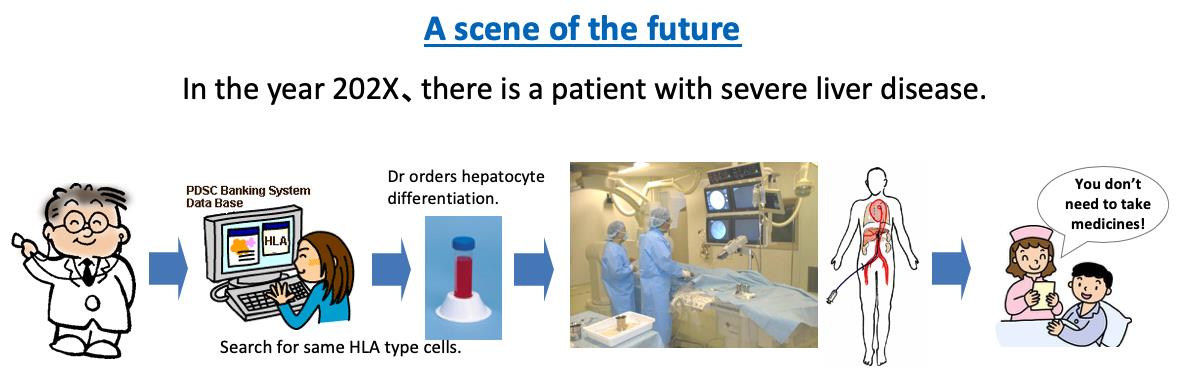
<羊膜上皮細胞を用いた細胞治療の臨床応用>
私たちは、ヒト胎盤から分離できる羊膜上皮細胞に幹細胞様の多分化能があることを発見しました(Miki T, et al. Stem Cells, 2005)。また、羊膜上皮幹細胞は肝臓内に移植することによって肝細胞に分化することがわかりました(Marongiu F, et al. Hepatology, 2011)。羊膜上皮細胞は、一つの胎盤から大量に分離できること、免疫原性が少なく、癌化の可能性も低いことなどから、私たちはこの羊膜上皮幹細胞を肝移植に代わる細胞治療の新たなソースとして利用できると考えています。すでに私たちは、先天性代謝疾患モデル動物を使った前臨床研究を行い、比較的少量の細胞移植で臨床症状の改善が見られることを示しました(Rodriguez N, et al. Stem Cells Trans. Med, 2017)。私たちは、この研究を発展させ臨床応用を目指したトランスレーショナル研究を行っています。