HOME > 糖尿病研究について > 糖尿病における最近の話題 > 糖尿病治療におけるグルカゴン分泌制御の重要性
はじめに
グルカゴンの主な生理作用は、肝臓のブドウ糖産生を増加させ、血糖値を上昇させることです。そのため、低血糖時のインスリン拮抗ホルモンとして認識されてきましたが、糖尿病においてグルカゴン分泌の調節異常が注目されるようになってきました。糖尿病では食前における血漿グルカゴン濃度の上昇、さらに食後における血漿グルカゴン濃度の抑制不全(あるいは上昇)がみられます。糖尿病における食後高血糖にはインスリン分泌不全とグルカゴン過剰分泌とが等しく寄与しているという報告があります。最近、グルカゴン分泌に注目した糖尿病治療が重要となってきています。
グルカゴンの分泌
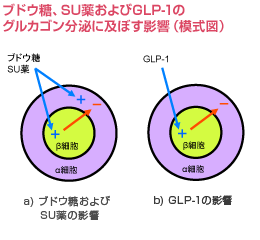
ブドウ糖あるいはSU薬が健常な膵島に作用した場合は、α細胞に対する直接のグルカゴン分泌促進作用は、β細胞を介する間接的な抑制作用で打ち消され、グルカゴン分泌は抑制される。しかし、 β細胞の数と機能が低下している2型糖尿病の膵島に作用した場合は、グルカゴン分泌を促進する可能性がある。一方、GLP-1はα細胞に対する分泌促進作用がないため、効率よくグルカゴン分泌を抑制する。
ブドウ糖をはじめとする栄養素や各種ホルモンによるグルカゴン分泌制御のメカニズムに関して未だ定説はありません。ここでは主流と思われる見解や私たちの研究室のデータに沿って解説します。健常者にブドウ糖の静脈注射を行うと血漿グルカゴン濃度は低下(グルカゴン分泌の抑制)します1, 2, 3)。
ブドウ糖はα細胞を直接刺激してグルカゴン分泌を促進させますが、同時にβ細胞やδ細胞からグルカゴン分泌抑制因子(インスリン、ソマトスタチン、GABA、亜鉛イオンなど)も分泌させます。ブドウ糖のα細胞への影響を総和した結果はグルカゴン分泌の抑制として表れ、抑制因子の作用が刺激作用よりも強いためと考えられます(図 a)。インスリン分泌の低下している糖尿病患者では、ブドウ糖の静脈注射によるグルカゴン分泌の抑制の程度が小さくなります1, 2, 3)。私たちはブドウ糖によりβ細胞から分泌される亜鉛イオンがパラクライン機構によりα細胞からのグルカゴン分泌を抑制することを発見し、現在そのメカニズムの研究を行っています4)。
ブドウ糖と同様に、スルホニル尿素薬もβ細胞やδ細胞からのグルカゴン分泌抑制因子を刺激すると同時に、α細胞に対してはATP感受性カリウムチャネルの閉鎖による直接刺激作用を持っています(図 a)。健常者にスルホニル尿素薬を投与すると、間接的なグルカゴン分泌抑制作用が強くグルカゴン分泌は抑制されますが、インスリン分泌のない1型糖尿病患者においてはα細胞への直接刺激作用がやや強くなり、血漿グルカゴン濃度は上昇する傾向にあります5)。
食事による血漿グルカゴン濃度の変化は、食事成分やインクレチン(消化管から分泌され、インスリン分泌を刺激するホルモン)によりさらに複雑な制御を受けます。高蛋白食では健常者と糖尿病患者のいずれにおいても、血漿グルカゴン濃度は上昇します6, 7)。それはアミノ酸がグルカゴン分泌を直接刺激するからです。高炭水化物食における血漿グルカゴン濃度の変化は健常者と糖尿病患者では異なります。これにはインクレチンであるglucose-dependent insulinotropic polypeptide(GIP)とglucagon-like peptide-1(GLP-1)が関与しています。GIPは食事により上部消化管のK細胞から血液中に分泌され、β細胞やδ細胞からの分泌を刺激する(グルカゴン分泌の間接的抑制)と同時に、グルカゴン分泌も直接刺激すると考えられています。健常者にGIPを静脈注射すると、グルカゴン分泌の刺激作用と抑制作用が相殺され、血漿グルカゴン濃度はほとんど変化しません8)。一方、GLP-1は下部消化管のL細胞から分泌され、β細胞やδ細胞の分泌を刺激することにより間接的にグルカゴン分泌を抑制すると考えられています(図 b)。α細胞への直接作用は現在のところ否定的です。健常者にブドウ糖や高炭水化物食を経口負荷すると血漿グルカゴン濃度は減少しますが、糖尿病患者では減少しないか、かえって上昇します6, 7)。2型糖尿病患者の血中GLP-1とGIPの血中濃度は健常者と同等であることより、消化管から分泌されるこれらのホルモンの量も健常者と同等と考えられます2)。ところが、2型糖尿病患者にブドウ糖と薬理量のGLP-1を同時に静脈から投与するとグルカゴン分泌は抑制されます。同様にブドウ糖とGIPを同時に投与するとグルカゴン分泌が刺激されます9)。以上の結果より、これらのホルモンが消化管から分泌される条件下において、糖尿病患者ではGIPのα細胞に対する作用がGLP-1の作用より強くなっていると推測されます。糖尿病状態になるとGIPのインスリン分泌作用(β細胞への作用)が低下し10)、グルカゴン分泌作用(α細胞への直接作用)が増強していると推測される現象は興味深いところです。今後の詳細な検討が必要です。
ところで、健常者と糖尿病患者の両者において高炭水化物食における血漿グルカゴン濃度は、ブドウ糖静注時にみられる濃度よりも高くなります。食事により消化管からはインクレチン以外の未知のホルモンも分泌されていると推測されます。それらのホルモン作用の総和はグルカゴン分泌を刺激する方向に作用するようです。インクレチン以外でグルカゴン分泌を刺激する消化管ホルモンとして、glucagon-like peptide-2(GLP-2)が挙げられています9)。
- 1) Meier JJ et al., Diabetologia. 2007; 50: 806-13.
- 2) Knop FK et al., Diabetologia. 2007; 50: 797-805.
- 3) Hare KJ et al., Am J Physiol. 2010; 298: E832-7.
- 4) Ishihara H et al., Nat Cell Biol. 2003; 5: 330-5.
- 5) Cooperberg BA et al.,Diabetes Care. 2009; 32: 2275-80.
- 6) Ahmed M et al., Am J Clin Nutr. 1980; 33: 1917-24.
- 7) Kawai K et al., Endocrinol Jpn. 1987; 34: 745-53.
- 8) Ahrén B et al., Diabetes Res Clin Pract. 1991; 13: 153-61.
- 9) Lund A et al., Am J Physiol. 2011; 300: E1038-46.
- 10) Vilsboll T et al., Diabetologia. 2002; 45:1111-1119.
グルカゴンの作用
グルカゴン受容体は種々の組織(心、消化管、腎、脳、脂肪組織など)に発現しており、これらの組織におけるグルカンゴンの様々な作用が知られています(表)。消化管蠕動運動の抑制作用は、消化管のX線及び内視鏡検査の前処置に臨床応用されています。グルカゴンの主な作用は、肝においてグリコーゲン分解と糖新生によるブドウ糖の産生・放出を促進し、血糖を上昇させることであり、これは低血糖時の救急処置に応用されています。健常者の空腹時において、グルカゴンはグリコーゲン分解により血糖値を上昇させます。一方、カテコラミンなどのインスリン拮抗ホルモンが上昇している状態(低血糖時やコントロール不良の糖尿病など)では、糖新生の基質が血液中に豊富となり、糖新生による血糖値上昇が優位となります11)。
肝臓 | 増加:グリコーゲン分解,糖新生,脂肪酸化,肝細胞生残性 減少:グリコーゲン合成 |
|---|---|
| 膵島 | インスリン分泌増加 |
| 消化管 | 腸蠕動抑制 |
| 心臓 | 陽性変力作用,解糖・ブドウ糖酸化増加 |
| 腎臓 | 糸球体濾過量増加,水再吸収増加 |
| 脂肪細胞 | 脂肪分解促進 |
| 中枢神経 | ブドウ糖産生,食欲抑制 |
- 11) Lecavalier L et al., Am J Physiol. 1990; 258: E569-75.
糖尿病における血漿グルカゴン濃度とその影響
血糖値の調節に最も関与しているホルモンはインスリンと考えられていますが、グルカゴンの作用もそれに劣らず重要です。最近、糖尿病においてグルカゴン分泌の調節異常が注目されるようになってきました。糖尿病患者の空腹時血漿グルカゴン濃度は健常者より上昇し、肝の糖産生による空腹時高血糖の原因となっています12)。さらに、1型糖尿病におけるケトアシドーシスはインスリンの枯渇だけでは誘導されず、グルカゴンによるグリコーゲン分解、糖新生、ケトン体生成、および脂肪分解が関与します13)。
食事やブドウ糖負荷後において肝の糖吸収を促進させる因子としてもインスリンが重要とされていますが、グルカゴンはインスリンのこの作用に対しても拮抗的に働きます。糖尿病患者における食後の血漿グルカゴン濃度の上昇(抑制不全)は、肝グリコーゲン合成の低下と肝糖産生の不十分な抑制をもたらし、食後高血糖につながります14)。筋肉におけるブドウ糖の取り込み量は健常者との差はみられません。食後の高グルカゴン血症は、膵炎やステロイドによる糖尿病でも観察されていますので、高血糖状態でみられるインスリン抵抗性などによる2次的な現象と考えられています15)。
- 12) Dunning BE et al., Endocr Rev. 2007; 28: 253-83.
- 13) Gerich JE et al., N Engl J Med 1975; 292: 985-9.
- 14) Krssak M et al., Diabetes. 2004; 53: 3048-56.
- 15) Hansen KB et al., J Clin Endocrinol Metab. 2011; 96: 447-53.
インクレチンおよびその関連薬によるグルカゴン分泌抑制作用と血糖改善効果
糖尿病患者にGLP-1を注射すると食後の過剰なグルカゴン分泌が抑制され、食後高血糖の改善がみられます。血漿グルカゴン濃度は、 2型糖尿病において約50%、1型糖尿病において約20%まで低下します16)。GLP-1投与による2糖尿病患者の治療において、グルカゴン分泌の抑制作用による血糖降下度とインスリン分泌促進作用による血糖降下度は同程度であるという報告があります17)。一方、2型糖尿病患者において、食事負荷時にGIPを投与すると、血漿グルカゴン濃度が上昇し、血糖値も軽度上昇します18)。従って、GIPは血糖コントロールという面においては糖尿病治療薬として適さないと考えられています。
現在、2型糖尿病の治療において2種類のGLP-1アナログ製剤が使用されていますが、いずれの製剤も食後の血漿グルカゴン濃度を低下させることが報告されています。また、臨床研究レベルでは内因性インスリン分泌が枯渇した1型糖尿病患者でも同様の作用が報告されています。この結果は、GLP-1の刺激によりδ細胞から分泌されたソマトスタチンがグルカゴン分泌を抑制することを示唆しています。
- 16) Gutniak M et al., N Engl J Med. 1992; 326: 1316-22.
- 17) Hare KJ et al., Diabetes. 2010; 59: 1765-70.
- 18) Chia CW et al., Diabetes. 2010; 58: 1342-9.
- 19) Foley JE et al., Horm Metab Res 2008; 40: 727-30.
終わりに
最近まで、高血糖の原因としてインスリン分泌不足のみが強調されていました。ところが、GLP-1関連薬の登場を契機にグルカゴンの高血糖への関与が注目され始め、グルカゴンの分泌や作用に関する研究が盛んに行われるようになってきています。今後の糖尿病の治療は、インスリンとグルカゴンの両者の血中濃度を制御することを目的とした方向へ進むと考えられます。グルカゴンについて現在までの研究成果を簡単にまとめましたが、未だ不明な部分が数多く残されています。当教室ではグルカゴン分泌とその作用について、基礎的・臨床的側面の両方から研究を進めています。